5 जुलाई को, नोवो नॉर्डिस्क ने चीन में कैग्रीसेमा इंजेक्शन का तीसरे चरण का क्लिनिकल परीक्षण शुरू किया, जिसका उद्देश्य चीन में मोटे और अधिक वजन वाले रोगियों में सेमग्लूटाइड के साथ कैग्रीसेमा इंजेक्शन की सुरक्षा और प्रभावकारिता की तुलना करना है।
कैग्रीसेमा इंजेक्शन नोवो नॉर्डिस्क द्वारा विकास के तहत एक लंबे समय तक काम करने वाली संयोजन चिकित्सा है, मुख्य घटक जीएलपी -1 (ग्लूकागन-जैसे पेप्टाइड -1) रिसेप्टर एगोनिस्ट स्मेग्लूटाइड और एक लंबे समय तक काम करने वाले एमाइलिन एनालॉग कैग्रिलिंटाइड हैं।कैग्रीसेमा इंजेक्शन को सप्ताह में एक बार चमड़े के नीचे लगाया जा सकता है।
प्राथमिक उद्देश्य कैग्रीसेमा (2.4 मिलीग्राम/2.4 मिलीग्राम) की सप्ताह में एक बार चमड़े के नीचे सेमेग्लूटाइड या प्लेसिबो से तुलना करना था।नोवो नॉर्डिस्क ने स्टेज 2 मधुमेह के इलाज के लिए कैग्रीसेमा के परीक्षण के परिणामों की घोषणा की है, जिससे साबित हुआ कि कैग्रीसेमा का हाइपोग्लाइसेमिक प्रभाव सेमेग्लूटाइड से बेहतर है, और लगभग 90% विषयों ने एचबीए1सी लक्ष्य हासिल कर लिया है।
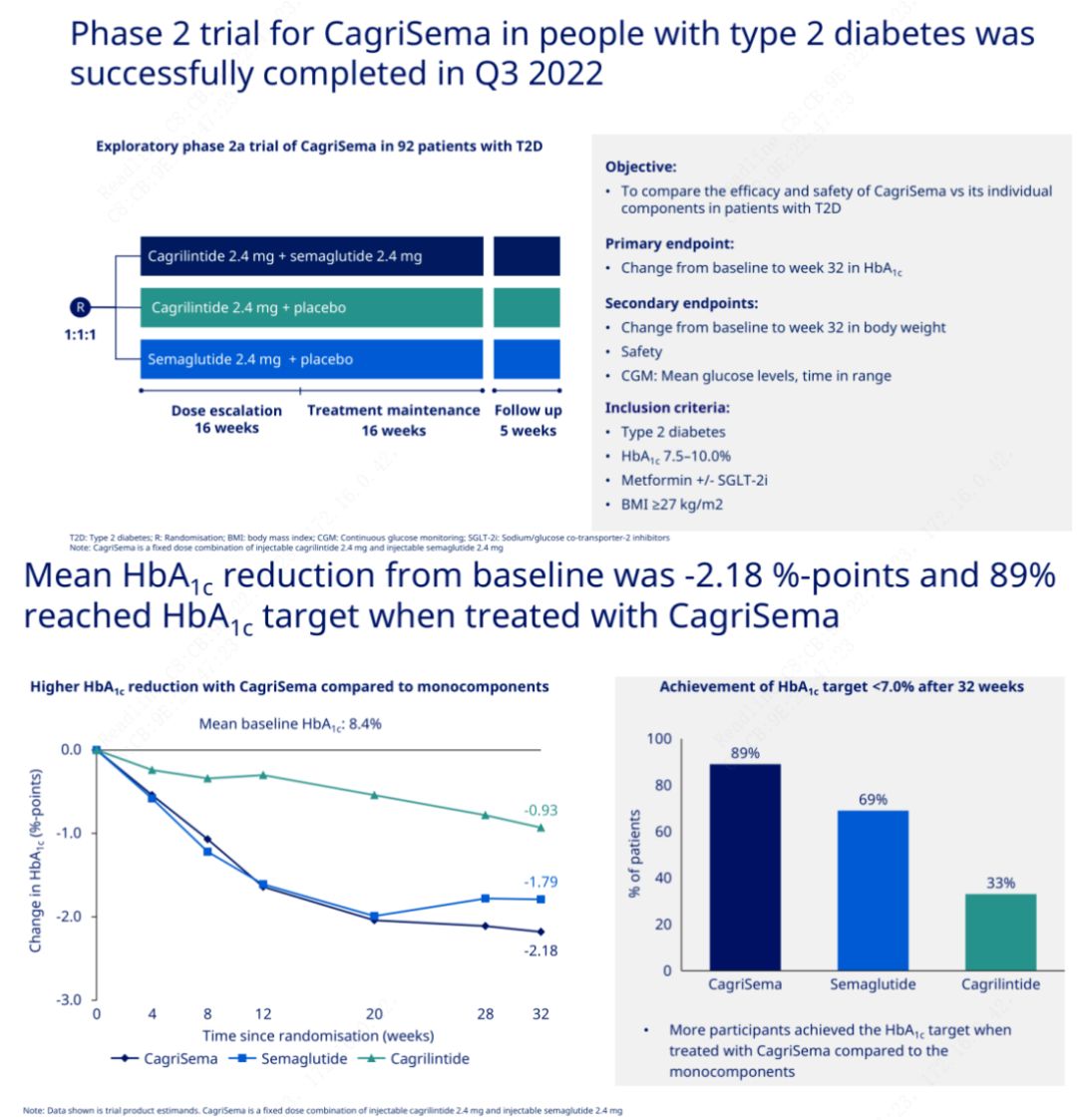
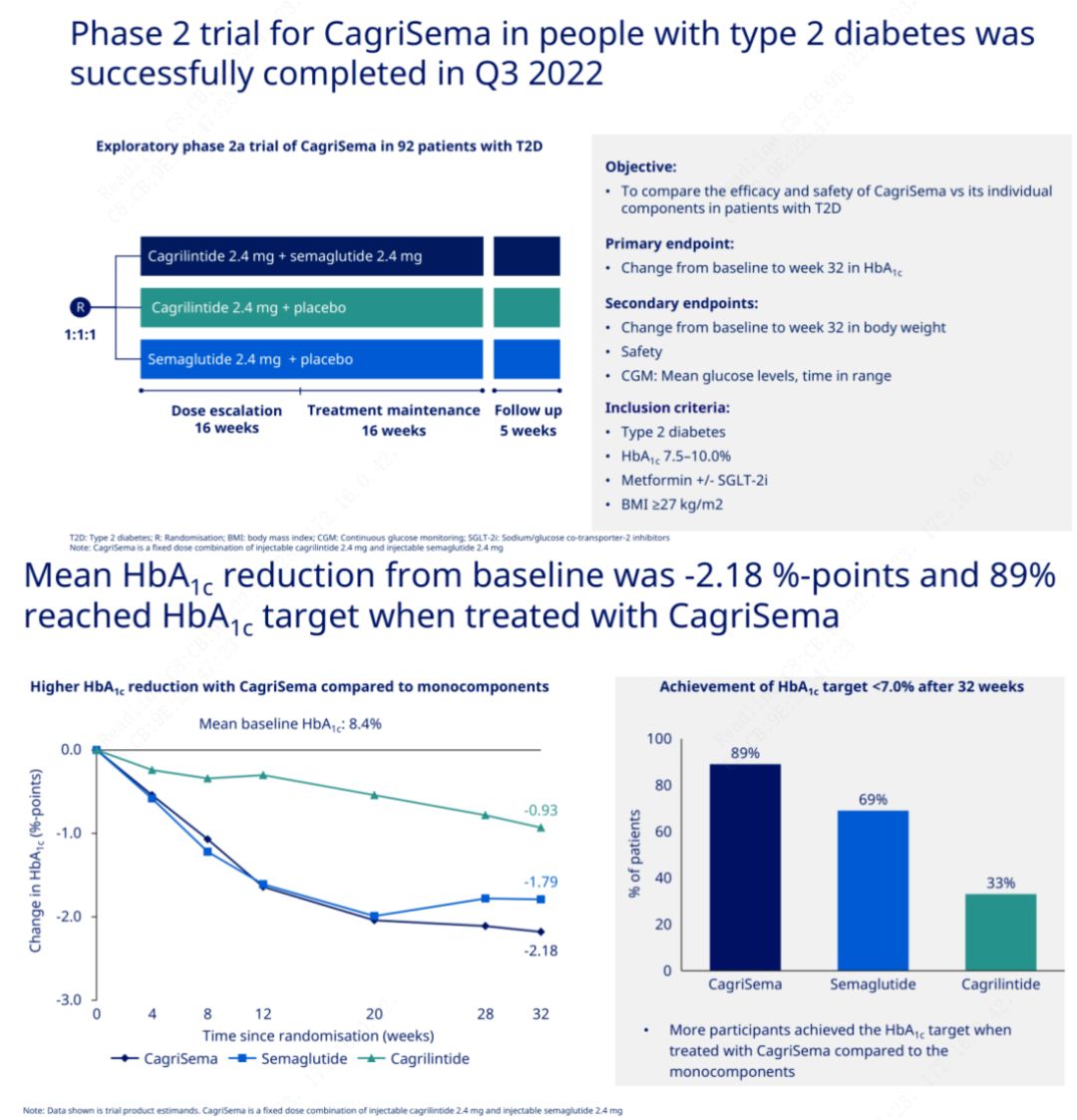
डेटा से पता चला है कि महत्वपूर्ण हाइपोग्लाइसेमिक प्रभाव के अलावा, वजन घटाने के मामले में, कैग्रीसेमा इंजेक्शन ने 15.6% वजन घटाने के साथ सेमेग्लूटाइड (5.1%) और कैग्रिलिंटाइड (8.1%) से काफी बेहतर प्रदर्शन किया।
नवोन्मेषी दवा तिरजेपेटाइड दुनिया की पहली अनुमोदित साप्ताहिक जीआईपी/जीएलपी-1 रिसेप्टर एगोनिस्ट है।यह दो इन्क्रीटिन के प्रभावों को एक एकल अणु में जोड़ता है जिसे सप्ताह में एक बार इंजेक्ट किया जाता है और यह टाइप 2 मधुमेह के लिए उपचार का एक नया वर्ग है।टाइप 2 मधुमेह वाले वयस्कों में ग्लाइसेमिक नियंत्रण (आहार के आधार पर और व्यायाम पर) में सुधार के लिए मई 2022 में अमेरिकी खाद्य एवं औषधि प्रशासन (एफडीए) द्वारा तिरजेपेटाइड को मंजूरी दे दी गई थी और वर्तमान में इसे यूरोपीय संघ, जापान और अन्य देशों में मंजूरी दे दी गई है।
5 जुलाई को, एली लिली ने टाइप 2 मधुमेह रोगियों के उपचार के लिए दवा नैदानिक परीक्षण पंजीकरण और सूचना प्रकटीकरण मंच पर चरण III SURPASS-CN-MONO अध्ययन की घोषणा की।SURPASS-CN-MONO एक यादृच्छिक, डबल-ब्लाइंड, प्लेसबो-नियंत्रित चरण III अध्ययन है जिसे टाइप 2 मधुमेह वाले लोगों में प्लेसबो की तुलना में टिरजेपेटाइड मोनोथेरेपी की प्रभावकारिता और सुरक्षा का मूल्यांकन करने के लिए डिज़ाइन किया गया है।अध्ययन में टाइप 2 मधुमेह वाले 200 रोगियों को शामिल करने की योजना बनाई गई थी, जो विजिट 1 से पहले 90 दिनों में किसी भी एंटीडायबिटिक दवा पर नहीं थे (कुछ नैदानिक स्थितियों को छोड़कर, जैसे गंभीर बीमारी, अस्पताल में भर्ती, या वैकल्पिक सर्जरी, अल्पकालिक (≤14) दिन) इंसुलिन का उपयोग)।
इस वर्ष टाइप 2 मधुमेह को मंजूरी मिलने की उम्मीद है
पिछले महीने, SURPASS-AP-कॉम्बो अध्ययन के नतीजे 25 मई को ब्लॉकबस्टर जर्नल नेचर मेडिसिन में प्रकाशित हुए थे।परिणामों से पता चला कि इंसुलिन ग्लार्गिन की तुलना में, तिरजेपेटाइड ने एशिया-प्रशांत क्षेत्र (मुख्य रूप से चीन) में टाइप 2 मधुमेह रोगियों की आबादी में बेहतर एचबीए1सी और वजन में कमी दिखाई: एचबीए1सी में 2.49% तक की कमी और वजन में 7.2 किलोग्राम तक की कमी आई। (9.4%) 40 सप्ताह के उपचार में, रक्त लिपिड और रक्तचाप में महत्वपूर्ण सुधार हुआ, और समग्र सुरक्षा और सहनशीलता अच्छी थी।
SURPASS-AP-कॉम्बो का चरण 3 क्लिनिकल परीक्षण तिरजेपेटाइड का पहला अध्ययन है जो मुख्य रूप से टाइप 2 मधुमेह वाले चीनी रोगियों में आयोजित किया गया है, जिसका नेतृत्व पेकिंग यूनिवर्सिटी पीपुल्स हॉस्पिटल के प्रोफेसर जी लिनॉन्ग ने किया है।SURPASS-AP-कॉम्बो अनुसंधान की वैश्विक SURPASS श्रृंखला के परिणामों के अनुरूप है, जो आगे साबित करता है कि चीनी रोगियों में मधुमेह का पैथोफिज़ियोलॉजी वैश्विक रोगियों के अनुरूप है, जो नई दवाओं के एक साथ अनुसंधान और विकास का आधार है। चीन और दुनिया में, और चीनी रोगियों को नवीनतम मधुमेह उपचार दवाओं और चीन में उनके नैदानिक अनुप्रयोग को जल्द से जल्द उपयोग करने का अवसर देने के लिए ठोस साक्ष्य समर्थन भी प्रदान करता है।
पोस्ट करने का समय: सितम्बर-18-2023

